 Créditos:
Créditos:
A diretoria colegiada da Agência Nacional de Vigilância Sanitária (Anvisa) aprovou por unanimidade nesta sexta-feira (22) o segundo pedido de uso emergencial da CoronaVac. Agora, a autorização é válida para as doses envasadas no Brasil.
As duas áreas técnicas presentes na deliberação, a coordenação de Inspeção e Fiscalização de Insumos Farmacêuticos e a gerência-geral de Medicamentos e Produtos Biológicos, também foram favoráveis à aprovação.
No último dia 17, a Anvisa autorizou o uso emergencial da vacina, mas a permissão era apenas para as doses importadas prontas da China.
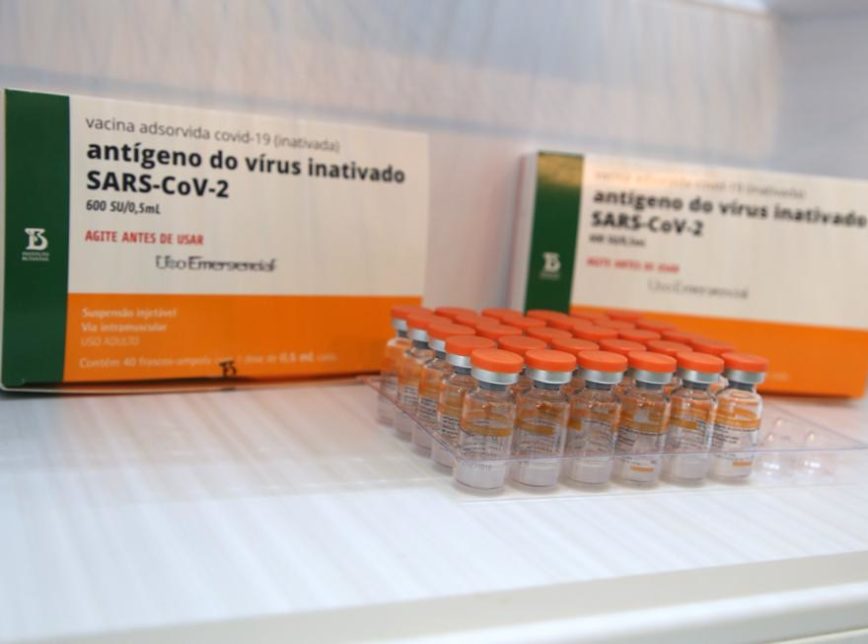
Desta vez, o Instituto Butantan pediu a aprovação da vacina em outra embalagem, do tipo frascos-ampola multidose — com dez doses em um só recipiente. No requerimento anterior, as doses vinham fracionadas.
A solicitação, realizada no dia 18, compreende 4,8 milhões de doses que estão prontas no instituto paulista e mais 35 milhões que estão em produção.
A diretora da Anvisa Meiruze Sousa Freitas afirmou que as análises não encontraram benefícios no aumento do intervalo entre as doses que superem os riscos. "O melhor cenário é ampliar o acesso às doses e manter o intervalo estabelecido na bula", disse.
Um estudo da desenvolvedora do imunizante, Sinovac Biotech, afirma que o estudo clínico no Brasil mostrou que a vacina foi mais eficaz em um sub-grupo que recebeu as doses com intervalo de 3 semanas.
Fonte: CNN